
南山区区委书记王强赴赛动生物调研,解决企业发展中的问题
2019年5月9日
国内首份《细胞储存产业发展研究报告》在深发布
2019年7月28日创新科技成果构建细胞治疗有效性指标评价体系

本文根据刘沐芸博士在“第十九届中南地区输血医学学术交流”上的演讲报告整理,演讲内容如下:
创新科技成果构建细胞治疗有效性指标评价体系
细胞产业发展概况:
国际:细胞治疗领域近年因其革命性应用前景和潜在市场需求,在生物领域异常亮眼。特别随着技术的进步,细胞治疗产业相关研究进入多元化发展阶段。围绕细胞的研究除了细胞治疗、组织器官移植修复、基因治疗之外,正朝着药物研发、毒理评估工具、发育生物学模型等领域扩展。
大家可以看得到,截至2019年1季度,据Alliance for Regenerative Medicine统计,全球共有906个以再生医学为主营业务的公司(包括细胞治疗、基因治疗、基因修饰的细胞治疗和组织工程产品开发)。北美484家、欧洲和以色列地区241家,亚洲地区142家等。大家可能会好奇,刚才有专家发言提到,仅深圳就有超过300家的细胞公司,这个统计数据怎么亚洲地区才142家公司?这是因为,该统计是将“向所在国监管部门提交了再生医学产品新药申请”作为入选指标。这一点提示我们,发展再生医学产业,需要符合行业的科学规律和客观路径。
截至2018年12月,全球已批复上市的细胞产品(包括基因治疗产品)共25个。国际细胞产品注册临床研究项目数总计1028项, I期341项,II期595项,III期99项。可以预见,在不久的未来,会陆续有适应症以肿瘤为主(58%)的细胞产品获批上市,进入临床使用。
国内:随着国外细胞技术的不断发展,我国相关政府部门也陆续出台了法律法规和指导原则,极大地促进了我国细胞产业的发展。党的十九大召开后,我国药品监督管理局大力改革新药审评审批制度,将细胞产品列入药品管理以来,重开了细胞新药申报的大门。在国家卫健委备案获得干细胞临床研究资格的医疗机构有103家,并有37个干细胞临床研究项目完成备案,获准正式开展干细胞临床研究,但细胞产品上市尚未实现零的突破。
近年来,不断有生命科学领域科学发现引发的基础突破,而催生的新理论、新技术、新工具的普及也进一步提升了我们对细胞产品安全性、有效性的认知水平、评价能力和审评效率。比如,组学、下一代测序、质谱分析等的方法和工具的出现,促发了精准医疗、靶向治疗等临床医学的进步,也提升了监管部门快速评价有效性的手段——用替代性标记快速评价新药是否有效等。
当然,这些新知识、新技术和新工具为细胞产品的研发、评价也提供了发展新思路、研发新路径和监管新方法。
输血是最古老的细胞治疗,所以输血行业发展、管理和评价的关键节点等的设置与细胞治疗具有高度重合性。这也是为什么,我国的监管部门将最早的脐带血造血干细胞库又称之为“特殊血站”的缘故,美国也是如此。AABB的前身是美国血库协会。所以,细胞治疗的安全性和有效型评价体系的构建可以借鉴我国输血行业的管理经验,并吸纳我国血液行业所经历过的一些经验和教训。
这也是为什么我会参加咱们血液系统年会的背景。我们单位对细胞制剂的安全性指标就是建立在输血行业的“血筛指标”的基础上,再结合细胞产品的具体特征制定完善。
但一个产品用到人身上,尤其是治疗药物,仅有安全是远远不够的,还必须要有效才行。
今天我的演讲题目是以科技创新成果来建立一个细胞治疗的安全有效性的评价体系,也就是以科技成果赋能企业研发和监管体系。那我就以比较通用型的间充质干细胞为例,探讨一下如何用创新的科技成果建立一个适配细胞产品“生物活性”特点的评价体系,也就是找到与其治疗适应症相关的分子标记(Indication Speicific Marker),优化细胞治疗的临床效果。
1.前言
间充质干细胞(英文缩写:MSCs)是一类存在于多种组织(如骨髓、脐带组织、胎盘蜕膜组织、牙髓、脂肪组织等),具有多向分化潜力,非造血干细胞的成体干细胞,来源广泛,并且容易分离扩增。
和造血干细胞类似,它在临床上发挥着重要的治疗作用,也是比较广为大众熟知的。但与造血干细胞不同的是,间充质干细胞不是通过功能的替代发挥临床治疗作用,而是通过旁分泌的作用发挥治疗效应。优点就是不需要配型,具有一定“广谱性”,不足就是不能向造血干细胞移植那样,定植体内后可以长期发挥其“生理职能”。
目前在美国国立卫生研究院(National Institutes of Health, NIH)临床数据库(ClinicalTrials.gov)注册的,与间充质干细胞相关的临床试验已涉及300多种疾病,与间充质干细胞相关的临床试验就多达到947项, 其中亚洲地区是295项。
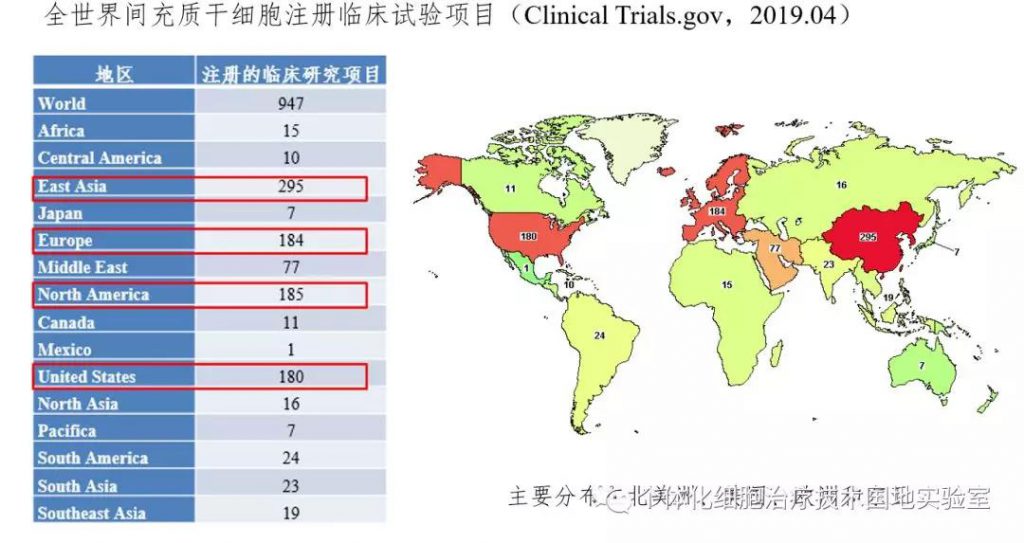
2.间充质干细胞注册的适应症非常广泛
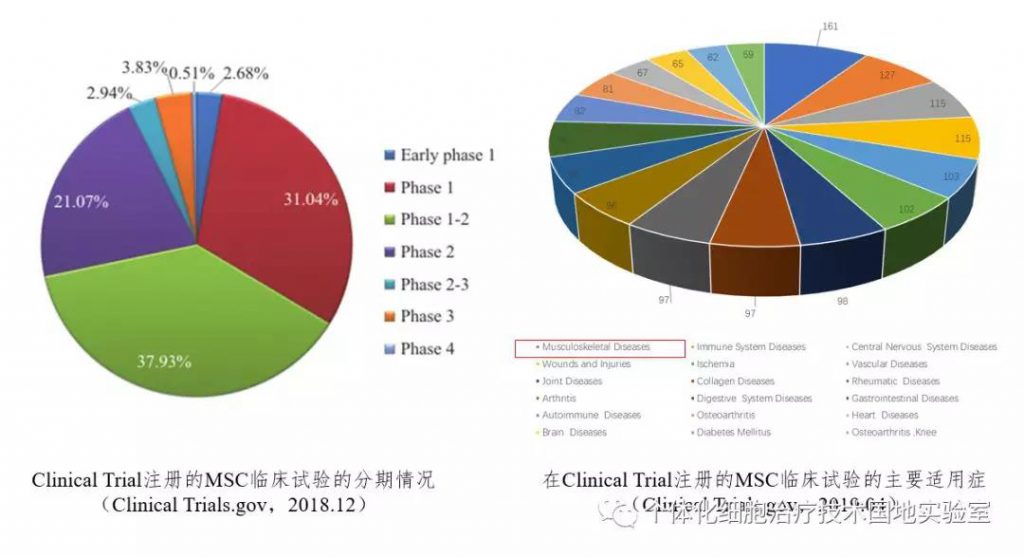
从上述图表可以看出,间充质干细胞注册的适应症是非常广泛的,包括肌肉骨骼疾病、中枢神经系统疾病、贫血、血管疾病、关节疾病、风湿性疾病、关节炎、消化系统疾病、肠胃疾病、自身免疫性疾病、骨关节炎、心脏疾病、脑部疾病、糖尿病骨、膝盖关节炎等等。然而间充质干细胞的应用过程中也逐渐暴露了一些问题:例如异质性(个体差异、来源差异、以及受体微环境的差异等),可塑性等。
异质性:不同个体来源的MSC,尽管基本特性相同(如形态、表面标志物、多向分化能力等),但其功能存在差异;同样,不同组织来源MSC 基本特性相同,功能各有千秋,然而目前缺乏监测MSC功能的质量标准,我们如何获得适合疾病治疗的MSC?
疗效差异:很多研究报告显示,不同的临床研究小组,用同一种间充质干细胞或者同一种来源的甚至同一种骨髓来源的间充质干细胞,治疗同一个适应症的时候,可能一个小组研究结果显示是非常好,但是另一个小组的结果显示不是特别好。
这说明当前常用的间充质干细胞通用评价指标不能满足MSCs研究进展的需求。目前通用的MSCs的评价指标只表明这是间充质干细胞,但与其需要治疗的具体的适应症就很难界定。
比如MSCs有一个评价指标是成软骨性,但如果这一批的MSCs是用于治疗自身免疫性疾病,这一项成软骨的特性鉴定是否还是必须、关键指标?
再比如,同一个供体不同组织来源的MSCs(如骨髓、脐带组织、胎盘蜕膜组织、牙髓、脂肪组织等),其功能是否会有差异?不同供体的MSCs的功能是否不同? 这些都是在开发间充质干细胞制剂的研究过程中亟待回答的问题。
可塑性:MSC功能的发挥有赖于疾病微环境的“赋能”,而微环境复杂、多样,导致MSC治疗效果存在差异。
在不同的炎症相关疾病中MSC作用存在差异,甚至在同一疾病的不同阶段呈现出相反的作用,这可能与机体病理微环境相关。研究表明MSC免疫调节作用与微环境相互作用,且炎症因子的种类与浓度与MSC免疫调节能力密切相关。
所以,我们在临床上怎么样才能确定哪一种间充质干细胞适合治疗某一种特定的适应症?安全有效治疗评价体系如何构建?据此,我们提出以下科学问题:如何提升MSC临床治疗效率——不仅安全而且有效?
(1)通过枢纽基因筛选与适应症相关的MSCs
除细胞形态、表面标志、分化能力外,从表达谱角度标定MSCs的生物学属性,为MSCs细胞制剂提供精准质控标准。目前MSCs缺乏生物学功能的评判指标;我们的分析还发现,MSCs对于炎症因子刺激,存在一系列关键的枢纽基因。这些基因参与了免疫效应的调控,也涉及应答性调整。这提示我们这些枢纽基因或许可以作为分子标志,筛选最佳治疗效能MSCs,以使得MSCs具有更稳定更显著的临床治疗效能。
(2)应用表达谱分析方法探索治疗机制
探讨MSCs与病理微环境的相互作用模式,发现MSCs治疗有效的细胞与分子靶点。来源不同个体的细胞(个体差异、不同细胞因子处理),通过表达谱分析MSCs的旁分泌效应,找出不同炎症状态差异基因表达及其功能,挖掘关键的枢纽基因,提示我们可以基于表达谱数据分析,探讨MSC与病理微环境的相互作用模式,发现MSC治疗有效的细胞与分子靶点。
以我们实验室的工作《间充质干细胞通过胰岛素样生长因子结合蛋白7(IGFBP7)介导免疫抑制减轻实验性结肠炎》为例,探讨如何科技创新成果赋能行业研发和评价体系。
首先,我们在mRNA水平和蛋白水平证实IGFBP7的在MSCs中高表达;接着利用RNA干扰技术,发现IFGBP7具有可干扰的特征,这就显示IGFBP7可以作为候选分子。先在体外实验,发现 IGFBP7具有显著促进MSCs介导的免疫调节的作用。接着在动物模型,我们重复出体外实验的结果。我们的研究表明IGFBP7可以作为MSCs治疗自身免疫性疾病相关的一个有效性评价指标。
3.讨论:创新科技成果构建细胞治疗有效性指标评价体系
随着生命科学和生物科技快速发展,新理论、新工具、新检测方法的更新迭代,人类的最基本特征就是知道如何利用工具提高我们的生存效率。因此如何将生命科学、生物科技、计算科学等领域中的新工具应用到细胞治疗的质量评价中?以提升细胞治疗的临床应用转化效率,保障细胞治疗的临床效果,实现科技创新成果与临床治疗手段的结合。
(1)利用表达谱数据筛选MSC新效应分子的策略可行、可靠
我们在申报适应症要对应相应的细胞亚型,就和我们输血一样,配好血型。我们要配好适应症特异标记,也就是MSCs应该区分不同的亚型,而不能“什么都能干(One-For-All)”。间充质干细胞作为新药申报时,安全有效性的指标,你该怎么构建?作为监管部门,安全性、有效性的指标该怎么评价?
MSCs在临床具有广阔的应用前景,相关的临床前研究及临床试验已经证实某些MSCs在治疗某些适应症是安全、有效的;但其治疗机制仍远未阐明。我们基于表达谱分析构建的MSCs适应症相关分子的方法具有可靠性;基于表达谱数据分析方法将有助于我们探讨MSCs与微环境相互影响的作用机制、鉴定MSCs不同亚型的对应功能和调控机制。
(2) 建立适合不同疾病治疗的特异性MSC标准,实现细胞精准治疗
现行的国际细胞治疗协会的标准是一个通用的最低标准,只是表明这个细胞是间充质干细胞,并不能将MSCs的功能与其申报的适应症进行关联。缺乏对其生物学功能的监测,这也是导致MSCs治疗效果不稳定,乃至研究失败的主要原因之一。显然,目前这个通用国际标准已经无法满足MSCs产品审评审批的要求。
现在美国FDA接受MSCs申报的时候,已经开始要求提供与适应症相关的功能性指标的研究结果了。那我们这个研究方法和成果是不是可以为MSCs国际标准的更新提供思路?现行的国际细胞治疗协会关于MSCs的评价标准,是不是到了要适应性调整的时候了?
通过大批量的MSCs表达谱数据分析,我们可以筛选适合不同疾病治疗的MSCs生物学指标,并建立适合不同疾病治疗的特异性MSCs标准,实现精准化治疗。
(3)建立MSCs分子标记数据库,实现个体化治疗
未来可以考虑建立大规模的MSCs细胞库,并获得MSCs的表达谱数据库。在这一个大规模库的基础上,一方面,我们可以将病人的个体特征与MSCs亚型信息库进行匹配,筛选适合个体应用的MSCs亚型;另一方面,我们也可以在治疗前提取病人的个人标本,如外周血,在体外与不同MSCs亚型进行配对筛选,以挑选出适合个体应用的最佳细胞株。
因此,我们可以利用表达谱数据筛选建立MSCs亚型分子库和数据库,不仅仅是为企业提供了提升细胞治疗新药研发效率的方法和路径,也为监管部门提供了一个很有效的评价工具和指标。
4.总结:创新科技成果提升细胞治疗效果
细胞治疗是个新兴的领域,它有很多我们还不太知晓的环节,正是因为很多不太知晓的,也为我们的研究也提供了很多的线索,我们可以开展许多具有针对性的研究,提供确定的证据在国家细胞标准领域形成我们的话语权。
大家都知道,现在可能每个地方,包括广东、海南、上海等多个地方政府,都非常支持细胞技术和产业的发展。
最后,我以深圳为例。谈谈如何支持一个新兴产业的发展。支持一个新兴产业的发展,不仅仅是政策的支持,还要在技术本身发展逻辑和科学规律方面有针对性地支持把关。
深圳是这样做的, 2013 年就将细胞技术列为未来产业重点培育发展,并于2014年设立《深圳市未来产业发展专项资金》实施“个体化细胞治疗‘创新链+产业链’融合专项”,该举措不仅关注细胞技术本身的突破与攻克,还充分关注到了“技术突破”到“临床工具”中间过程的关键环节和能力建设,甄别出细胞产业链中关键或缺失环节,作为弥补细胞产业关键缺失环节的细胞质量分析检测服务平台——成立了深圳科诺医学检验实验室,承担第三方的细胞质量检定职能,保障细胞储存和临床研究的安全性和有效性。
“魏则西”事件发生以后,深圳同期发布产业支持计划时,设立了第三方的一个免疫细胞质量分析的检测服务平台,以保障免疫细胞的安全性和有效性。所以深圳作为一个特区的城市,在支持新兴产业发展上,不仅仅是政策文件的支持,并结合了技术本身的特性,从产业逻辑和基本规律出发。
2018年9月,深圳市血液中心与个体化细胞治疗技术国家地方联合工程实验室共同成立的细胞质量监测技术联合实验室,就致力于突破细胞质量监测瓶颈,以细胞质量监测领域关键技术、共性技术为主要方向,重点进行细胞质量监测技术开发和标准规范建立,培养细胞质量监测技术人才,实现细胞质量监测相关技术的科研成果转化。将血液中心的存量技术体系和细胞实验室的创新研究成果进行结合,构建新技术孵化新产业的质量评价和保障体系。实验室在安全性的指标上面,结合血液系统传统优势的血筛这样的一套评价方法、指标和体系,以及我们细胞里面的一些特定的要求,形成了一套良好的细胞治疗的安全性评价体系。
今天介绍的内容,其实就是要表达一个观点,细胞治疗要发展形成一个新兴产业——科学承诺细胞质量是前提!质量设施的打造才是对产业尤其是生命健康产业的最大支持,基于行业的基本规律和产业逻辑,要懂得利用不断涌现创新科技成果的关键工具作用,用科技成果赋能监管手段,比如美国FDA就是应用了新一代测序技术找到了替代性标记实现了肿瘤药的快速审批。
充分发挥科技创新工具性作用,构建细胞治疗有效性指标评价体系,结合行业标准规范做好监管加法,才能切实发展出根基稳健的科技创新产业,增强人民群众从生物科技成果转化的获得感。维护公众健康,促进产业发展。
谢谢!
