
深圳女科技工作者,快来找组织啦~
2021年9月2日
加快再生医学疗法研发和上市的注册机制研究
2021年9月14日细胞治疗行业健康发展的几点思考
作者:任远 来源:国地
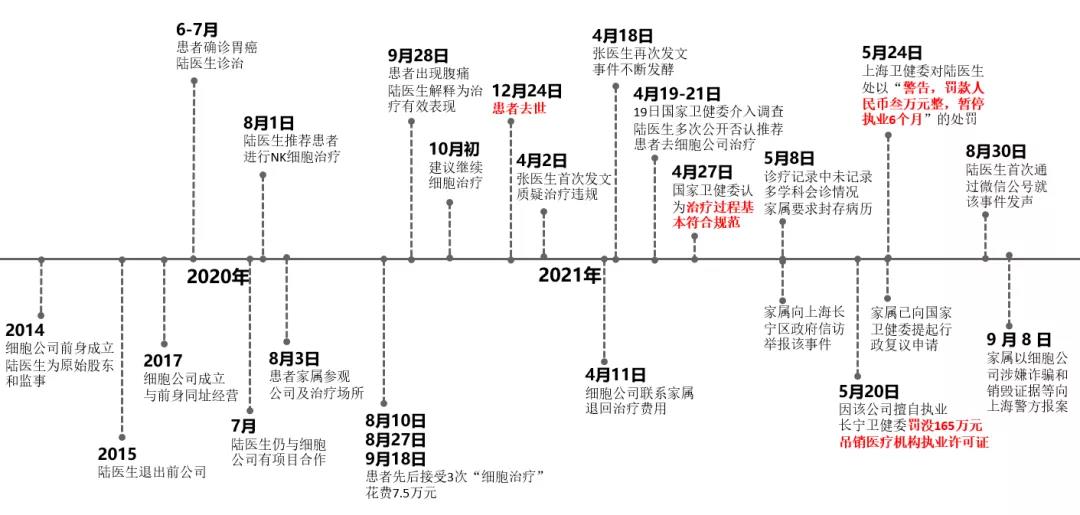
近日“肿瘤门”事件不断发酵,我们在此以时间轴的形式梳理了整个事件的来龙去脉(图一)。回顾过去,医疗机构开展细胞治疗,内地有“魏则西事件”,香港有“DR细胞医美事件”,这一系列事件让细胞治疗技术和产品质量成为关注焦点,将我国细胞行业推到了风口浪尖。
细胞治疗进入临床使用的质量如何保障、细胞行业该如何健康发展?我们在此行了分析和讨论。

图一、“肿瘤门”事件时间轴
一、消除大众认知盲点、严惩医疗机构过度宣传
一些机构或者企业扩大宣传细胞技术的疗效与安全性以吸引患者,导致了患者过高的预期值。民众普遍缺乏专业的宣传教育,正规医疗卫生机构和专业学会对细胞疗法的风险揭示和警示不足,形成了信息严重不对称。此外,监管机构的法规不严谨、政策不明晰或执行不到位,都会被不合格从业者加以利用。
二、建立规范标准,明确监管职责
加强质量认证体系建设,充分发挥质量认证保障安全底线,对涉及人身健康、安全环保的产品实行强制性认证。生物科技产业要想健康发展,行之有效的法案约束必不可少。需要明确规定,对于保障安全性和有效性的生产条件、生产工艺、质量体系是否达到人用产品的强制性要求。对于场地、软硬件和人员资质等出台明确技术细则,同时区分实验室技术和临床应用要求的本质差别。
针对我国目前在细胞治疗方面的规范不够完善、监管体制不够健全的现状,首要就是要加强立法和行政监管。规范化的标准有利于提高我国细胞治疗行业的民众信任度。责任明确的监管分工,可以减少空白监管区、消除重复监管区。厘清干细胞、免疫细胞等细胞制品制备过程中,哪些关键环节需要加强监管力度,弥补监管的盲点。
三、独立第三方细胞质量检测技术公共服务平台——以信息科技消除技术方与患者间的信息不对称
1、 好的研究成果从实验室到最终的商品化,除了基础研究和技术研发,还需要补齐完善整个转化链条上关键的职能。现行的法规里只规定了细胞库和区域细胞制备中心,包括临床机构的规范,但是缺乏了第三方的质量检测平台。从临床中常规实施的“三查七对”原则和药品生产过程中常规的“操作-复核-现场QA”GMP规范,都表明对细胞质量需要独立的第三方细胞质量检测平台把关,在制度和流程上对实施细胞技术临床研究和应用的项目和医院进行风险控制。
科诺医学检验实验室开放了一套可供细胞储户查询自己存储细胞是否合格的细胞质量查询系统。一方面实现自律,另一方面也通过信息科技和数字技术建立可行的行业体系,降低细胞领域中消费者与服务提供方之间的信息不对称,保障细胞安全。
四、加速从“细胞制造”到“细胞智造”转型
细胞制品的制备过程目前仍处于低效、高风险、产品不均一的手工制备生产线阶段,行业的手工、静态生产体系无法满足细胞治疗高复杂性的生产要求。因此,开发能符合小批量、多批次、高质量和动态监测需求的,数字化、自动化、在线实时监测的智能、柔性生产线就显得非常迫切。
赛动智造提供的“一键启动”细胞智造无人生产线(CellAuto-StemCell Platform)是这一问题的根本解决方案,它“按下”了我国细胞生产智能化、数字化的转型键。
1、 细胞智造无人生产线将人工智能和生物科技相结合,搭建细胞行业数字化、智能化的无人全自动细胞智造系统,可降低对“熟练工”的依赖。在提升当前手工细胞制备产量的同时,也能够保障批间质量的一致性。

细胞治疗作为一种全新的治疗手段,为人类战胜肿瘤、自身免疫疾病、新型突发传染病等重大疾病提供了全新的思路,有望成为人类延续生命、提高生存质量的最佳手段之一。
当研究突破来临时,我们需要用“科技+标准”做好细胞行业质量监管。除了细胞药物的研究开发,细胞产品稳定合格交付还需要产业设施建设(细胞库、制备中心、第三方检测中心、高端装备研究生产等),中间环节关键能力建设(关键工程人才、围绕着合格产品生产的供应链建设、CRO、CDMO等),政策、标准、法律法规(生命科学、生物科技和产业发展的配套金融体系和监管路径)等一系列产业关键共性软、硬能力和设施。
