
赛动智造:以智能质造赋能生物医学新技术安全转化
2025年9月22日
破局细胞分割难题:赛动智造创新算法引领精准分割新纪元
2025年12月17日新政落地!干细胞 “放行时代”来临,赛动智造以合规科技筑牢产业基石

2025 年 10 月 11 日,国务院总理李强签署国务院令,《生物医学新技术临床研究和临床转化应用管理条例》正式公布,这一重磅政策标志着干细胞技术从科研探索迈向规范化临床应用的 "放行时代" 已然来临。在这场关乎生命健康的产业变革中,"合规" 成为贯穿科研与转化全链条的核心命题,而临床研究记录与原始材料的规范化管理,则是守住合规底线的关键所在。
此次新规用专条明确了临床研究记录管理的刚性要求,条例原文如下:
第二十二条:临床研究机构应当及时、准确、完整记录生物医学新技术临床研究实施情况,留存相关原始材料。记录和原始材料应当自临床研究结束起保存30年;临床研究涉及子代的,记录和原始材料应当永久保存。临床研究发起机构、临床研究机构不得伪造、篡改、隐匿生物医学新技术临床研究记录和原始材料。
这与 2022 年国家药监局《细胞治疗产品生产质量管理指南(试行)》中 "细胞产品关键追踪记录或资料,至少保存三十年" 的要求一脉相承,共同构筑起细胞技术安全应用的制度屏障。
政策的密集出台绝非偶然。近年来,细胞治疗领域的违规事件时有发生,济南某医院擅自开展未获批NKT免疫细胞治疗的案例警示我们:缺乏规范的数据管理与追溯体系,不仅会让患者健康陷入风险,更会阻碍整个产业的健康发展。新规的落地,正是为产业发展划定了清晰的合规路线图。
作为细胞全生命周期管理领域的先行者,深圳赛动智造科技有限公司早以政策为导向,构建起覆盖科研、生产全流程的合规管理体系,让数据合规从 "被动应对" 变为 "主动防控"。
iTrustTracking(可信研发项目管理系统),将 "真实有效" 嵌入实验记录的每一个环节,每次实验记录均需电子签名确认,从源头杜绝研究数据造假可能。
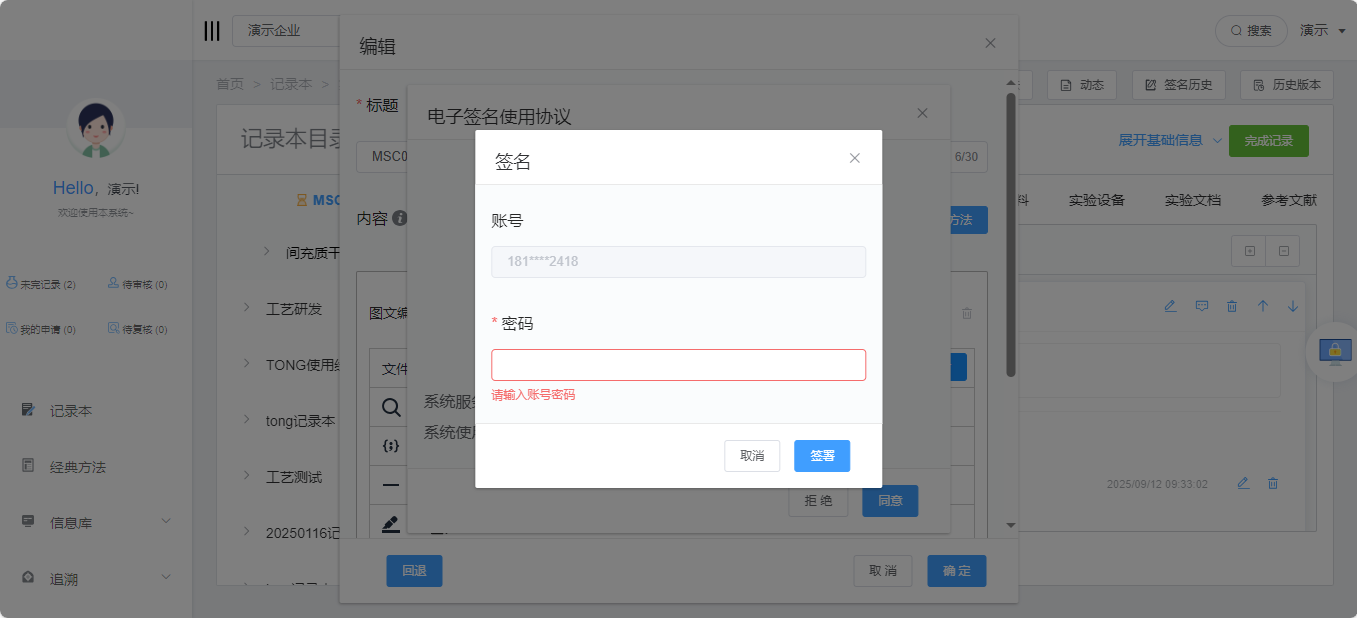
图:实验记录电子签名
MES(细胞生产执行系统),建立 "数据权限管控" 的刚性机制:所有生产记录、送检记录、检测记录、送存记录、废弃记录等支持权限管控、电子签名。原始数据永久留存、不可物理删除,完全满足新规 "及时、准确、完整" 的核心要求。
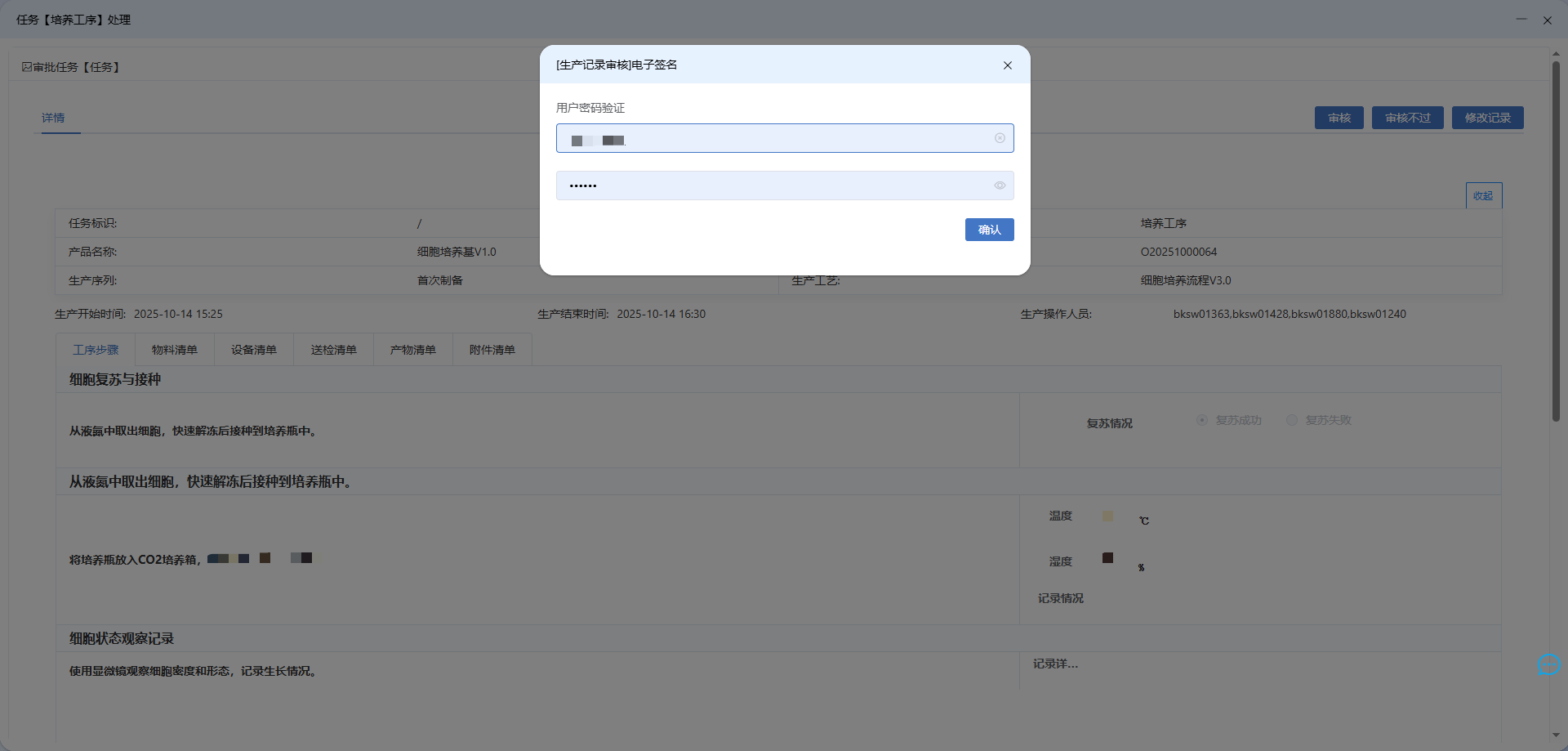
图:生产记录审核
更值得关注的是,平台打通了各系统的数据链路,内置全方位日志模块,科研操作、生产流程、质量检测等每一步动作都可追溯审计。这种 "全程可回溯" 的设计,恰是对政策要求的精准响应,让合规核查有据可依。
在数据可查可溯的基础上,赛动智造自主研发的CTS(细胞追溯系统),通过专利级追溯体系架构与全生命周期数据模型,串联医院端、物流端、企业端数据,实现了细胞产品从供者到患者、从患者到供者的双向精准追溯。这一功能不仅让供者材料、关键物料的追溯管理变得高效便捷,更让每一份细胞产品都拥有了清晰的 "身份档案",完美契合政策对关键追踪记录的管理要求。
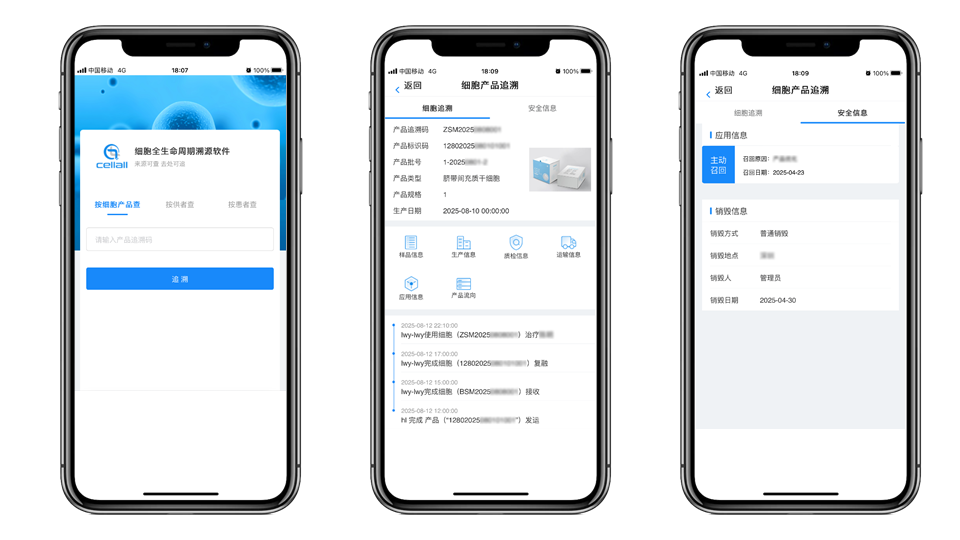
图:细胞产品追溯信息查询
从科研记录的电子认证到生产数据的全程留痕,从原始材料的永久保存到细胞产品的双向追溯,赛动智造以全链条合规管理能力,为企业搭建起应对政策监管的 "安全网"。
干细胞技术被视为继药物治疗、手术治疗后的"第三次医学革命",其临床转化的每一步都关乎生命健康与产业未来。当《生物医学新技术临床研究和临床转化应用管理条例》为产业发展 "放行",合规能力已成为企业核心竞争力的重要组成部分。
赛动智造细胞全生命周期管理平台,以政策为纲、以科技为刃,将 30 年保存、数据保真、双向追溯等合规要求转化为可落地的技术方案。在这场产业升级的浪潮中,赛动智造已与全国多家细胞企业,医院达成合作,落地细胞全生命周期管理平台,以合规科技赋能创新,让细胞技术在规范轨道上加速转化,真正实现了"让老百姓用得起、用得上、用得明白"的产业愿景。
合规之路,科技护航。赛动智造与您共赴细胞治疗的黄金时代!
